Cụ thể, Cục Quản lý Dược mới đây đã có Công văn số 1223/QLD-CL về việc thông báo thu hồi dung dịch nhỏ mắt Tobradico.
Nội dung văn bản nêu, căn cứ Công văn số 76/VKNTTW-KHTH ngày 7/2/2023 của Viện Kiểm nghiệm thuốc Trung ương về thuốc Dung dịch nhỏ mắt Tobradico (Tobramycin (dưới dạng Tobramycinsulfat) 15mg/5ml), Số GĐKLH: VD-19202-13, Số lô: 0031022, NSX: 02/10/2022, HD: 2/10/2024 do Công ty CP Dược Khoa sản xuất.
Mẫu thuốc do Viện Kiểm nghiệm thuốc Trung ương lấy tại Công ty TNHH Đại Bắc (quầy 214, tầng 2, Hapu Medicenter, Số 1 Nguyễn Huy Tưởng, Thanh Xuân, Hà Nội). Mẫu thuốc không đạt tiêu chuẩn chất lượng về chỉ tiêu Thử vô khuẩn, vi phạm chất lượng mức độ 2.
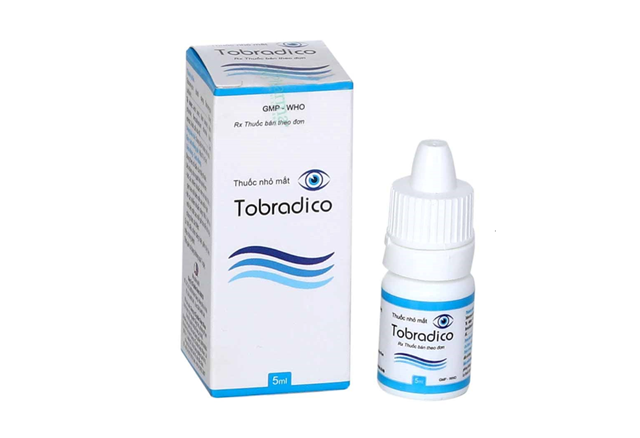
Theo đó, Cục Quản lý Dược thông báo thu hồi toàn quốc Dung dịch nhỏ mắt Tobradico (Tobramycin (dưới dạng Tobramycin sulfat) 15mg/5ml), Số GĐKLH: VD-19202-13, Số lô: 0031022, NSX: 2/10/2022, HD: 2/10/2024 do Công ty CP Dược Khoa sản xuất.
Cục Quản lý Dược yêu cầu Công ty cổ phần Dược Khoa phối hợp với nhà phân phối thuốc gửi thông báo thu hồi tới các cơ sở bán, sử dụng dung dịch nhỏ mắt Tobradico nêu trên và tiến hành thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng, gửi báo cáo thu hồi về Cục Quản lý Dược.
Ngoài ra, Cục Quản lý Dược cũng đề nghị sở y tế các tỉnh, thành phố và y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc không đạt chất lượng BM.CL.10.05/02 nêu trên; công bố thông tin về quyết định thu hồi thuốc trên trang thông tin điện tử của sở; kiểm tra và giám sát các đơn vị thực hiện thông báo này; xử lý những đơn vị vi phạm theo quy định hiện hành.
Sở Y tế Bắc Ninh cũng được yêu cầu thực hiện kiểm tra và giám sát Công ty cổ phần Dược Khoa thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.
Trước đó, Cục Quản lý Dược cũng đã phát đi thông báo thu hồi 11 lô thuốc Myomethol (Methylcarbamol 500mg) điều trị đau lưng do co thắt cơ, được nhập khẩu từ Thái Lan vì không đạt tiêu chuẩn chất lượng.
Cụ thể, nội dung thông báo cho biết, căn cứ Công văn số 80/CV-TTKN đề ngày 29/12/2022 của Trung tâm Kiểm nghiệm tỉnh Bình Dương báo cáo về kết quả kiểm nghiệm bổ sung chỉ tiêu Tạp chất liên quan theo quy định tại Dược điển Mỹ (USP 42) đối với 31 lô thuốc Myomethol (Methylcarbamol 500mg), số đăng ký VN-17397-13, do công ty RX. Manufacturing Co., Ltd – Thái Lan sản xuất, Công ty cổ phần xuất nhập khẩu y tế Tp. Hồ Chí Minh (YTECO) nhập khẩu, gửi kèm 11 phiếu kiểm nghiệm đối với 11 mẫu thuốc Myomethol (Methylcarbamol 500mg), số đăng ký VN17397-13, các mẫu thuốc được kiểm tra chất lượng bổ sung theo quy định về chất lượng thuốc nguyên liệu làm thuốc và không đạt tiêu chuẩn chất lượng BM.CL.10.05/02 về chỉ tiêu tạp chất liên quan Methocarbamol isomer.
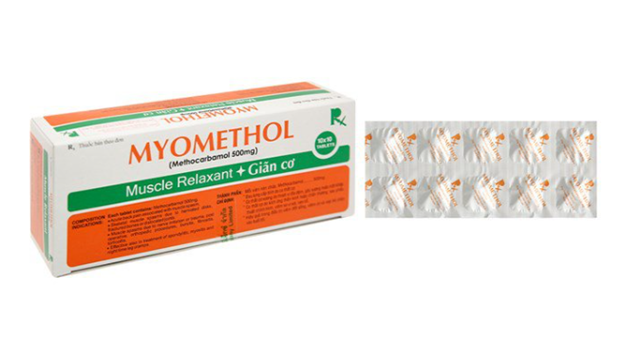
Vì vậy để đảm bảo an toàn cho người sử dụng, Cục Quản lý dược thông báo thu hồi toàn quốc 11 lô thuốc Myomethol (Methylcarbamol 500 mg) số đăng ký VN-17397-13.
Thuốc Myomethol bị thu hồi thuộc:
Số lô: 49U001, NSX 12.1.2021, HSD 12.1.2024
Số lô 49U002, NSX 12.1.2021, HSD 12.1.2024
Số lô 49U003, NSX 13.1.2021, HSD 13.1.2024
Số lô 49U004, NSX 13.1.2021, HSD 13.1.2024
Số lô 49U005, NSX 14.1.2021, HSD 14.1.2024
Số lô 49U006, NSX 14.1.2021, HSD 14.1.2024
Số lô 49U007, NSX 15.1.2021, HSD 15.1.2024
Số lô 49U008, NSX 4.2.2021, HSD 4.2.2024
Số lô 49U009, NSX 4.2.2021, HSD 4.2.2024
Số lô 49U010, NSX 5.2.2021, HSD 5.2.2024
Số lô 49U011, NSX 5.2.2021, HSD 5.2.2024
Cục Quản lý dược yêu cầu Công ty YTECO phối hợp với nhà phân phối gửi thông báo tới các cơ sở bán buôn, bán lẻ, sử dụng thuốc về việc thu hồi 11 lô thuốc Myomethol (Methylcarbamol 500mg) nêu trên và tiến hành thu hồi toàn bộ các lô thuốc không đạt chất lượng.
Sở Y tế các tỉnh, thành, y tế các ngành thông báo cho cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc không đạt chất lượng nêu trên; kiểm tra và giám sát các đơn vị thực hiện thông báo này; xử lý những đơn vị vi phạm theo quy định hiện hành.
Cục Quản lý dược cũng yêu cầu Sở Y tế TP.HCM kiểm tra và giám sát Công ty YTECO thực hiện việc thu hồi và xử lý các lô thuốc vi phạm theo quy định.
Sở hữu trí tuệ
In bài viết